PIF服務
PIF Service
產品資訊檔案 (PIF),您準備好了嗎
什麼是PIF
PIF,又稱為產品資訊檔案(Product Information File),是一份記錄化粧品產品品質、安全性與功效依據的檔案,確保產品安全性與有效性。
根據《化粧品衛生安全管理法》第4條規定,所有符合一定規模的製造或進口化粧品業者,在產品「供應、販賣、公開陳列或提供試用」前,必須完成:
- 線上產品登錄
- 建立PIF檔案
- 由具資格安全評估人員簽署安全報告
為什麼需要作PIF?
由於過往的化妝保養品沒有產品履歷、也沒有公開透明可查詢平台來確認產品真實性。強化業者自主管理及提升產品品質,進而保障化粧品消費安全,並與國際接軌,現在需於產品銷售前建立「化粧品產品登錄制度」,並同時開放民眾上網查詢任何一個上市產品資料,若沒有查詢到該產品資料或產品資訊不符均可向主管機關檢舉(檢舉成功還能領獎勵金)。
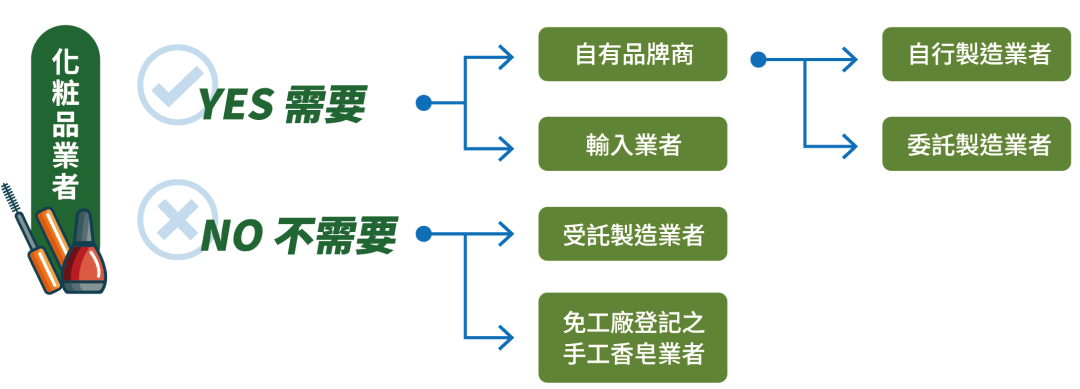
誰會需要建立PIF?
化粧品製造、輸入或販賣業者。化粧品業者需依法設立公司或商號、工廠及其他或製造輸入化粧品之團體或法人;免工廠登記之固態手工香皂業者除外。
PIF實施日期


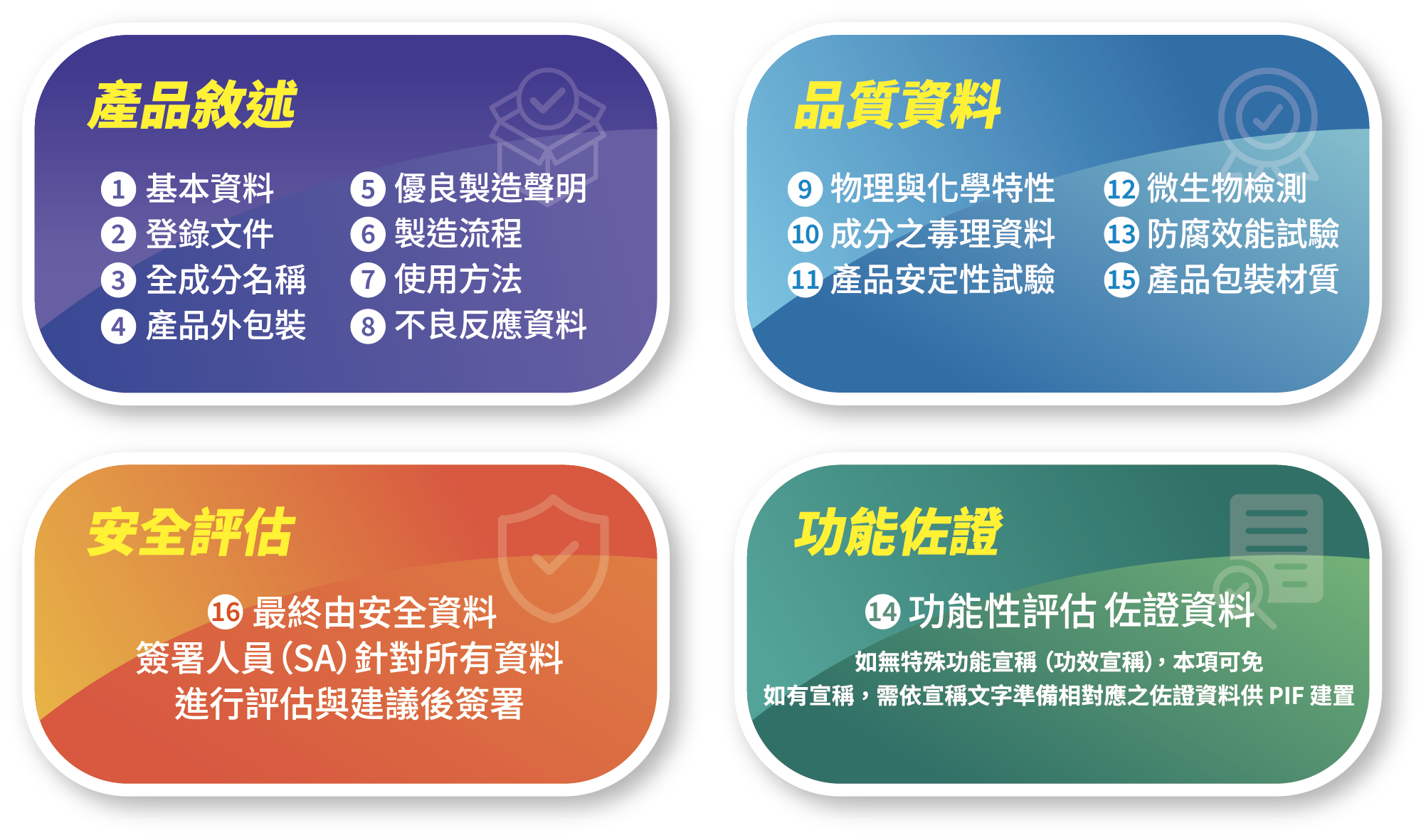
PIF應建立檔案內容

化粧品產品資訊 PIF 常見困擾
Q: 登錄產品之有效期限?
A: 產品登錄效期為3年,效期屆滿前3個月內須辦理展延登錄。
Q: 化粧品產品資訊檔案(PIF)保存方式?
A: 化粧品產品資訊檔案(PIF)應以書面或電子儲存方式保存,並自產品最後上市日之次日起,至少保存五年。
Q:PIF第9項「各別成分之物理及化學特性」原廠無法完整提供會不會影響案件進行?
A:不會影響,若無法完整提供各別成分CoA或SDS文件,SA人員將會參酌其他佐證文件進行評估。
Q:國外原廠很多文件無法提供到位,PIF報告還能簽署嗎?
可以,SA人員可依據現行文件內容進行評估,資料未詳盡之處可以論述方式加以說明。
Q:微生物試驗、防腐效能試驗及安定性試驗,若原廠資料無法使用怎麼辦?
可委託第三方實驗室進行成品檢測。
PIF未建置的罰則與法律風險
別輕忽!PIF不是形式作業,未建置將面臨重大罰則與市場風險:
違規行為 | 法條依據 | 罰則/處分內容 |
未建置產品資訊檔案(PIF)或內容不符規定 | 化粧品衛生安全管理法 第 28 條 | 處新台幣 1 萬元至 100 萬元 罰鍰,並得 按次連續處罰 |
經主管機關命限期改善,仍未改善 | 化粧品衛生安全管理法 第 29 條 | 得命 停止製造、輸入或販售,並得要求 下架回收;情節重大者,得 撤銷相關登記或許可 |
未完成化妝品產品登錄即上市販售 | 違反化妝品產品登錄相關規定 | 每一產品處 新台幣 6,000 元至 30 萬元 罰鍰 |
偽造、變造或虛構產品成分、試驗或相關文件資料 | 化粧品衛生安全管理法 第 8 條、第 21 條 | 得命 停產、停賣;若致危害人體健康,可能涉及刑事責任 |
化妝品檢驗
化粧品長期接觸肌膚,成分安全與功效性尤為重要。ATM艾特盟提供專業檢測,降低過敏風險,確保產品符合標準。 檢驗項目包含:
- 微生物與重金屬檢測:確保產品無受致病菌之汙染,篩檢鉛、汞、鎘、砷等重金屬,防止污染。
- 防腐劑與禁用成分:分析對羥基苯甲酸酯等酯類防腐劑,避免違規使用。
- 安全性與功能性評估:貼膚試驗、防曬係數測試、美白與抗菌成分分析,確保功效。
- 環境賀爾蒙與塑化劑:檢測雌激素、塑化劑等,降低內分泌干擾風險。
- 藥物與酸類成分篩檢:識別特定用途藥物、對苯二酚、酸類成分,防止違法添加。
ATM 艾特盟,專注產品安全與法規合規,協助品牌穩健提升市場競爭力。
一站式解決方案 | 常見需求專案服務項目
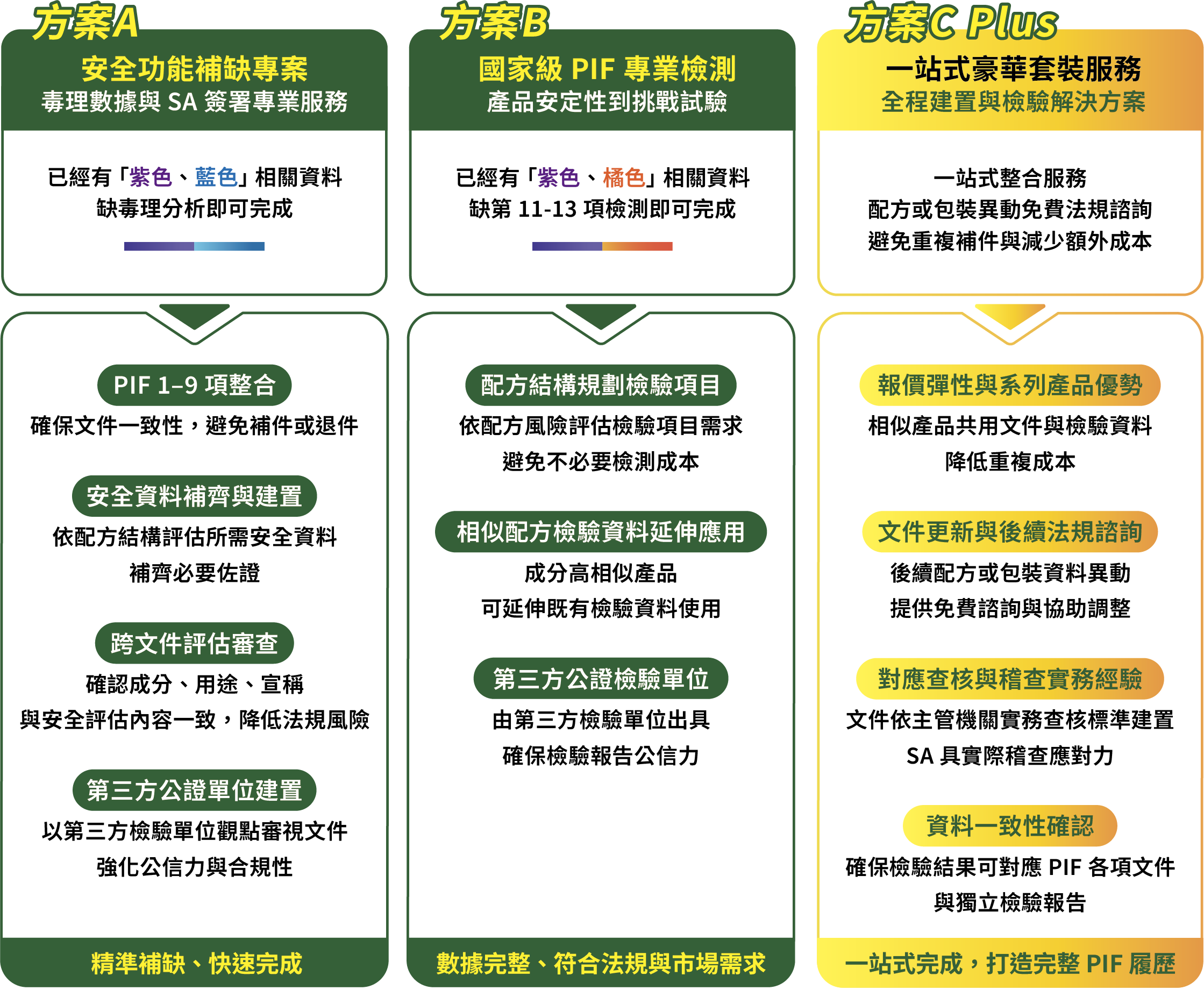
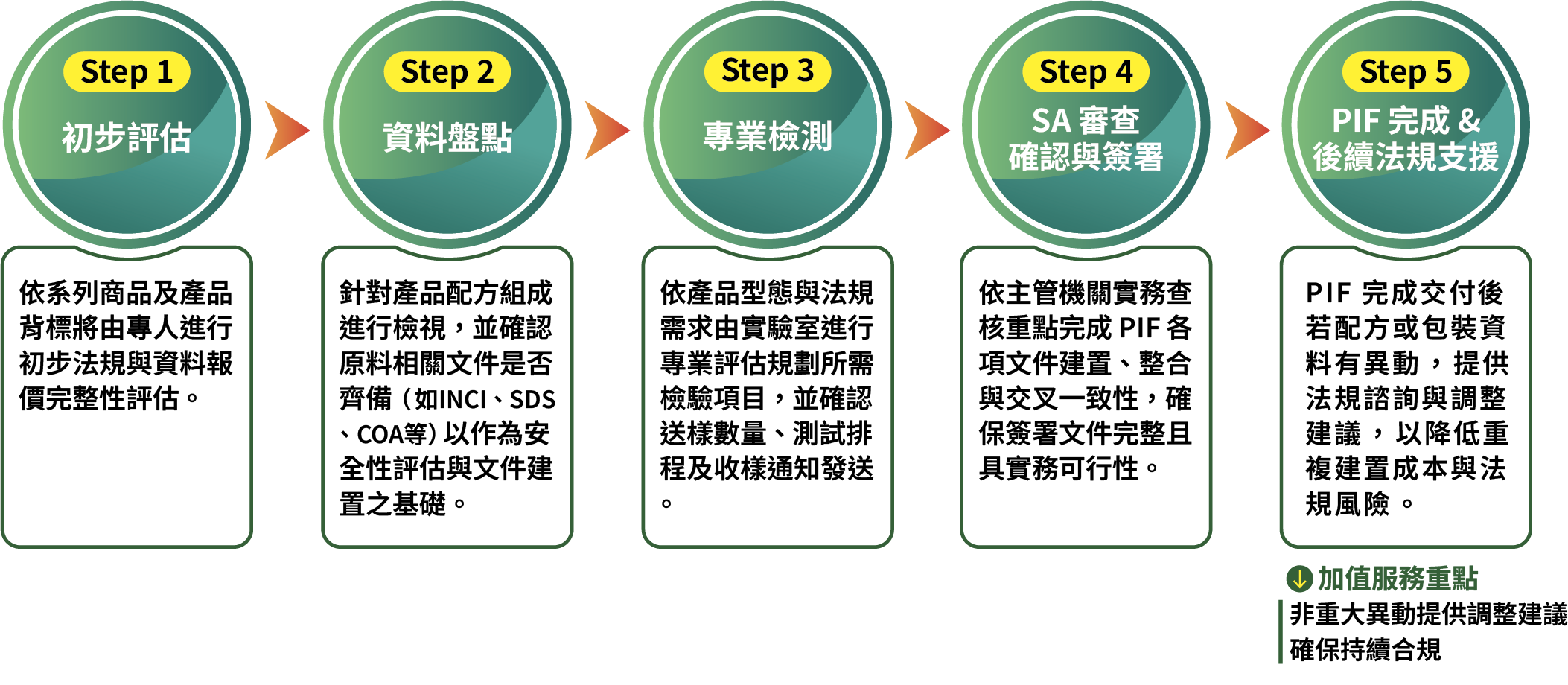
ATM PIF AI智能流程助您高效合規
PIF檢驗 / PIF法規上路您準備好了嗎?
什麼是PIF
針對各類化粧品進行毒理資料檢索、安定性試驗、防腐效能試驗等,並經由專業SA人員評估後進行簽署,確保產品安全性與有效性,降低皮膚過敏與健康風險,符合國際法規標準;我們特別提供 PIF(Product Information File)一站式檢驗服務,確保產品可合法上市並符合國際市場需求。
為什麼需要作PIF?
「一般化妝品」販售之產品登錄法規113年7月1日正式實施。自113年起,每件產品案件登錄、案件變更、案件展延,都將收取新台幣600元;且未完成登錄、違反登錄或產品資料不實者,也將處新台幣1萬元以上至100萬以下罰鍰,情節重大者得以停業、歇業或廢止營業許可等相關處分,切勿因小失大,為新法作好準備。
誰會需要建立PIF?

PIF實行時間
PIF應建立檔案內容

備註提醒:
PIF 文件非中文或英文建立者,應備有中文或英文譯本。
文件留存自產品最後上市日之次日起,至少保存五年。得以書面或電子檔,留存於中文標籤上標註之所在公司。
銷售期間進行任何變更,需隨時修正並經 SA 人員重新簽署。
*註3:依產品預估效期訂定儲存天數
*註4:每批產品都需進行成品微生物測試
*註5:觀察時間點須執行完整 28 天
一站式解決方案 | 常見需求專案服務項目

ATM PIF AI智能流程助您高效合規

PIF問題Q&A
哪些化粧品產品類別業者需要進行執行呢?
經衛生福利部公告之化粧品種類及一定規模之化粧品業者,包含依法設立的公司或商號、工廠及其他或製造輸入化粧品之團體或法人,都需建置PIF化妝品;免工廠登記之固態手工香皂業者除外。
化粧品產品資訊 PIF 是否需要將完整的 PIF 文件上傳到政府網站?
不用,業者只要以書面或電子儲存方式保存,存放於化粧品包裝上標示之製造或施入業者之地址,供主管機關備查。
化粧品產品資訊 PIF 需要保存多久?
自產品最後上市日之次日起,至少保存五年。
會公布讓消費者查閱嗎?因製造方法及流程涉及企業機密,是否有機密外洩之可能?
資料由業者以書面或電子儲存,無需上網登錄。
PIF 的建置責任,是由業者還是由代工廠負責?
依據「化粧品衛生安全管理法施行細則」第二條,化粧品產品登錄與產品資訊檔案建立應由化粧品製造或輸入業者為之。因此 PIF 建置應由化粧品製造或輸入業者負責。
化粧品如分段製造,是否只要列主要製造廠資料即可?
化粧品產品登錄何時實施?
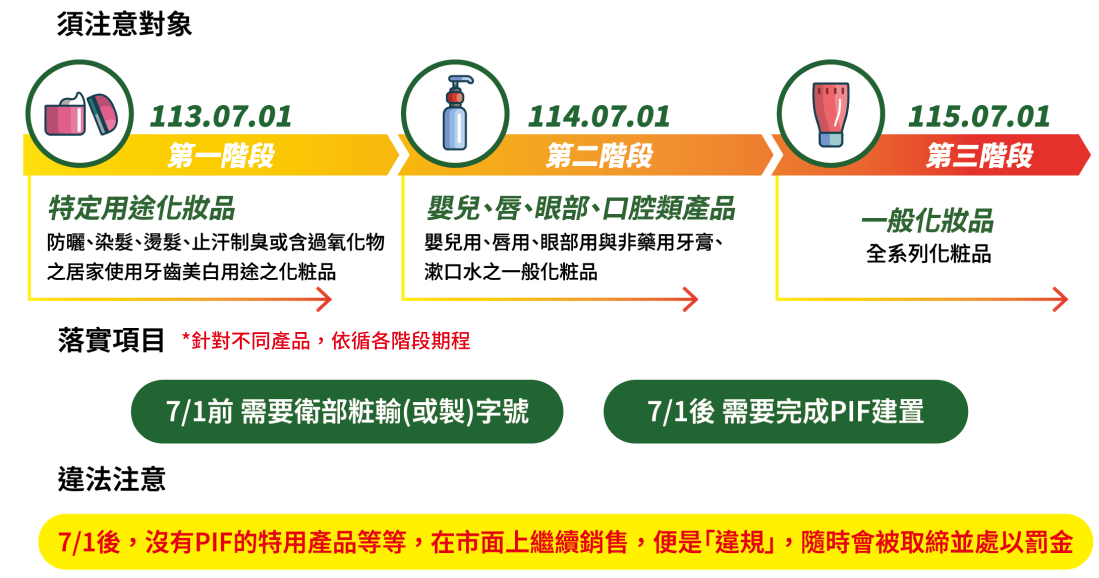
PIF/GMP準備期,何時正式實施?
1.特定用途化粧品自113年7月1日施行
2.嬰兒用、唇用、眼部用與非藥用牙膏、漱口水之一般化粧品自114年7月1日施行
3.前二點及免辦理工廠登記之化粧品製造場所生產之固態手工香皂以外之化粧品自115年7月1日施行
有效日期標示在標籤上的呈現方式?
應以壓印或不褪色油墨印刷、打印等方式,標示於外包裝、容器或標籤之上。以標籤為之者,其所有標示項目應以不褪色油墨,印刷或打印於同一張標籤,不得分別為之。
小體積、贈品、試用品標示方式及內容?
化粧品外包裝或容器最大之表面積小於40平方公分者,至少應標示品名、用途、製造或輸入業者之名稱、製造日期及有效期間,或製造日期及保存期限,或有效期間及保存期限。其他應標示事項,應標示於標籤、仿單、卡片、吊牌或說明書。另得以數位化形式公開應標示事項,並於外包裝或容器加刊可供辨識之二維條碼,以供民眾查詢。
字體大小規定?
(1)產品內容物淨重或容量大於800g或800mL者,字體高度及寬度均不得小於2.0mm。
(2)產品內容物淨重或容量小於(含)800g或800mL大於300g或300mL者,字體高度及寬度均不得小於1.6mm。
(3)產品內容物淨重或容量小於(含)300g或300mL者,字體高度及寬度均不得小於1.2mm。
產品如已登錄,是否一定要在產品外包裝標示其登錄字號?
考量國際管理趨勢,自110年7月1日起毋須標示許可證字號及登錄字號。